بقلم: ستيفان أليوس – رئيس قسم الدواجن العالمي
تنشر الهيئات الصحية الوطنية والإقليمية والدولية سنويًا تقارير حول انتشار الأمراض الحيوانية المنشأ. وتُعد السالمونيلا، والكمبيلوباكتر، والإشريكية القولونية من أبرز ثلاثة أمراض منقولة عبر الغذاء على مستوى العالم، حيث تتسبب في إصابة ملايين الأشخاص باضطرابات معوية قد تستدعي دخول المستشفى، وفي بعض الحالات تؤدي إلى الوفاة.
ترتبط نسبة من حالات الإصابة بهذه الأمراض الحيوانية المنشأ بقطاع الدواجن، وتحديدًا البيض أو لحوم الدواجن مثل الفروج (اللاحم) أو الديك الرومي. وعلى الرغم من أن التلوث بالسالمونيلا أو الكمبيلوباكتر لا يؤثر عادة على صحة الدواجن، فإن التلوث بالإشريكية القولونية غالبًا ما ينعكس سلبًا على صحة وأداء القطيع. وهذا يُعد مؤشرًا مبكرًا لمربّي الدواجن على وجود خطر متزايد قد يطال المستهلك، ويجب نقل هذا التحذير بوضوح عبر سلسلة الإنتاج. وبما أن الدواجن نادرًا ما تتأثر بالأنماط المصلية غير المتخصصة بالمضيف من السالمونيلا أو الكمبيلوباكتر، فإن السبيل الوحيد لتقدير مستوى الخطر هو عبر المراقبة المستمرة لوجود هذه البكتيريا في الدواجن وخلال مراحل الإنتاج المختلفة. وبفضل اللوائح الصارمة التي وضعتها السلطات الوطنية، تم تحقيق تقدم كبير في هذا المجال خلال العقود الماضية. ومع ذلك، لا تزال هذه الأمراض قائمة رغم كل الجهود المبذولة.
السالمونيلا جزء من البيئة, لذا فإن وجودها دائم
بينما نسلّط الضوء في هذا المقال على السالمونيلا وداء السالمونيلا، من المهم التأكيد على أن بكتيريا السالمونيلا موجودة في البيئة بشكل عام، وأن الأنماط المصلية غير المتخصصة بالمضيف تُعد ممرضة للإنسان ولكنها لا تُسبب أمراضًا للدواجن. بل إن بعض هذه الأنماط تُعتبر مفيدة للنباتات، كونها تساهم في العمليات البيئية التي تحلل المواد العضوية المعقدة إلى جزيئات أبسط وأسهل امتصاصًا. وحتى في قطاع تربية الدواجن، يمكن لبعض الأنماط أن يكون لها تأثير إيجابي على الإنتاج. فإعادة تدوير المغذيات التي تسهم بها هذه البكتيريا تعزز خصوبة التربة وتدعم التفاعل الحيوي بين النبات والتربة. وهذا يفسر سبب انتشار السالمونيلا في كل مكان، وليس في الحيوانات فقط.
تستطيع بكتيريا السالمونيلا أن تعيش في ظروف قاسية وصعبة للغاية. فهي قادرة على النمو ضمن نطاق حراري يتراوح بين 5 إلى 46 درجة مئوية، شريطة أن يكون الرقم الهيدروجيني (pH) لوسط النمو 5.5 أو أكثر، وأن لا يقل النشاط المائي (Aw) عن 0.94. أما إذا انخفض الرقم الهيدروجيني عن 4.5، أو انخفض النشاط المائي عن 0.94، فإن النمو يصبح صعبًا. ولهذا السبب بالتحديد، عندما تتواجد السالمونيلا في الدواجن، فإنها تُرصد غالبًا في الأعور، حيث تكون درجة الحموضة والنشاط المائي أعلى. إن فهم أماكن وجود هذه البكتيريا ومسارات انتقالها يُعد أمرًا جوهريًا لوضع استراتيجية فعالة للحد من تلوث الدواجن بها وتقليل خطر الإصابة بداء السالمونيلا. وتُشكّل الطيور الحاملة للبكتيريا دون ظهور أعراض خطرًا كبيرًا على سلامة الغذاء، إذ إن طائرًا واحدًا مصابًا في القطيع قد يؤدي إلى انتشار واسع للسالمونيلا بين الطيور، خاصةً عند التعرض لضغوط مثل الاكتظاظ، أو أثناء الإمساك بالطيور، أو خلال عمليات النقل.
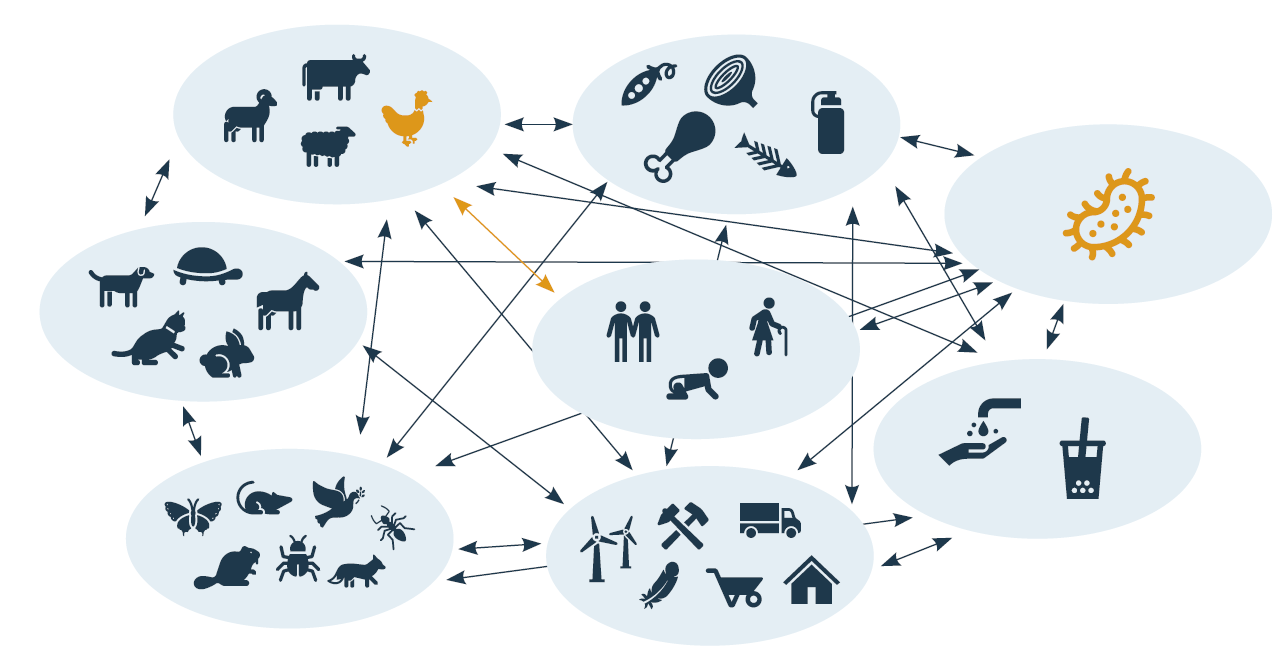
تتمتع خلايا السالمونيلا بالقدرة على البقاء حية رغم التجميد أو حتى الجفاف، من دون أن تفقد خصائصها الممرضة. كما يمكنها العيش في بيئات غنية بالأملاح. ومثلما زاد تغير المناخ من خطر وجود السموم الفطرية في الحبوب، فإن السالمونيلا قد تنتشر للأسباب ذاتها. فدرجات الحرارة المرتفعة وزيادة هطول الأمطار تهيئ الظروف المناسبة لبقاء السالمونيلا وتكاثرها بسرعة أكبر في الطبيعة. وبما أن السالمونيلا تشكّل جزءًا من التوازن البيئي الطبيعي، فإن مصادرها الطبيعية الأكثر شيوعًا تكون في المياه والتربة. وتتميز هذه البكتيريا بقدرتها على تكوين طبقة حيوية (biofilm) تحميها من الظروف القاسية أو من المواد المضادة للبكتيريا. إضافة إلى ذلك، تمتلك السالمونيلا آليات أخرى للبقاء، حيث تتنافس مع الكائنات الدقيقة الأخرى على العناصر الغذائية الأساسية، أو تتحرك باتجاه مواقع أكثر ملاءمة للبقاء والنمو والتكاثر، مثل استخدام عوامل الفوعة والقدرة على الغزو. ويُظهر الشكل 1 مسارات انتقال السالمونيلا المباشرة وغير المباشرة بين الحيوانات والإنسان، إلى جانب الآليات التي تمكّنها من البقاء والنمو والتكاثر داخل أجسام الحيوانات والبشر.
يُعد كسر مسارات انتقال العدوى أمرًا أساسيًا للحد من خطر الإصابة بداء السالمونيلا، ويمكن تحقيق ذلك إما من خلال تعزيز إجراءات الأمن الحيوي—مثل النظافة الشخصية، والتنظيف والتطهير المنتظم، ومنع دخول الطيور والقوارض، وعدم تربية الحيوانات الأليفة في مواقع التربية—أو من خلال تقليل إفراز السالمونيلا من الطيور المصابة، مما قد يساهم في منع تلوّث التربة أو المياه، وبالتالي كسر الحلقة المفرغة من التلوّث، والتلوّث المتبادل، وإعادة التلوّث.
كيفية تقليل خطر التلوث بالسالمونيلا
لا يهدف هذا المقال إلى استعراض إجراءات الأمن الحيوي التي يمكن اتباعها للحد من دخول السالمونيلا إلى سلسلة إنتاج الدواجن، بل يستعرض بشكل موجز استراتيجية فعالة لتقليل خطر السالمونيلا من خلال التركيز على الحيوان نفسه، وسلوك البكتيريا داخله.
تحديد عوامل الخطر .1
لحماية علامتك التجارية وتقليل احتمالية سحب منتجات لحوم الدواجن أو البيض من الأسواق بسبب داء السالمونيلا، من الضروري تطبيق برنامج مراقبة للكشف عن وجود بكتيريا السالمونيلا داخل عنابر التربية، وكذلك في البيئة المحيطة بوحدة الإنتاج. كما يجب تحديد مستوى خطر انتقال العدوى إلى الطيور داخل العنبر. تُظهر البيانات التحفظية أن أكثر من 4٪ من لحوم الدواجن والبيض حول العالم لا تزال تُسجّل نتائج إيجابية للسالمونيلا، مما يعني أن الوصول إلى “مخاطر صفرية” لا يزال غير ممكن. لذلك، فإن الخطوة الأولى تتمثل في تحديد النقاط الأكثر عرضة لوجود السالمونيلا داخل نظام التشغيل الخاص بك.
2. التركيز على تقليل عوامل الخطر في عملية الإنتاج
تتمثل الخطوة الثانية في التركيز على مصادر الخطر المحددة لتقليل احتمالية وجود السالمونيلا في جميع عناصر العملية الإنتاجية، بما في ذلك المعدات، والحيوانات، وعمليات المناولة، والمواد المستخدمة، وغيرها.
يختلف خطر وجود السالمونيلا في البيئة من منشأة إلى أخرى. فإذا كنت تعمل في منطقة استوائية رطبة قرب بحيرة، حيث تتردد الحيوانات البرية للرعي والشرب، فإن احتمالية وجود قوارض وحشرات ملوثة تحيط بعنبر الدواجن (وربما تدخل إليه) تكون أعلى بكثير مقارنة بمنطقة باردة نادرًا ما تتجاوز درجة حرارتها 10 درجات مئوية ولا توجد فيها مسطحات مائية قريبة. وقد أظهرت الدراسات أنه في تايلاند، تتراوح نسبة القطعان التي تُصاب بالسالمونيلا نتيجة القوارض والحشرات ما بين 49% إلى 75%.
وبالطبع، فإن أكبر مصدر خطر يتمثل في حال كان القطيع السابق مصابًا بالسالمونيلا، وبدأت بإفراغ الفرشة الملوثة من بيت الدواجن، خاصةً إن تم تخزينها لفترة قرب العنبر قبل التخلص منها. وهذا يُعد من الأسباب الرئيسية لانتشار السالمونيلا في بيئة المزرعة، وغالبًا ما يصعب السيطرة على البيئة الخارجية أو تنظيفها أو تطهيرها. ويكون خطر انتقال العدوى إلى نواقل التلوث كبيرًا في هذه الحالة، مما يشكل تهديدًا حقيقيًا للقطيع التالي عند دخوله إلى نفس العنبر.
3. السالمونيلا: من المصدر إلى الهدف – كيفية الحد من انتقال العدوى
الخطوة الأخيرة تتمثل في تعزيز مناعة الدواجن المعرضة لخطر التلوث بالسالمونيلا. فمن المعروف أن عمر الطائر وحالته الصحية العامة لهما تأثير كبير على احتمالية الإصابة. فعلى سبيل المثال، تكون الفروج اللاحم أكثر عرضة للإصابة خلال الأيام العشرة الأولى من العمر، نظرًا لعدم اكتمال كفاءة الجهاز المناعي الطبيعي. وبشكل عام، إذا أصبح القطيع السليم إيجابيًا للسالمونيلا، فإن ما بين 5% إلى 10% من الطيور تُصاب. أما في حال كانت الطيور مريضة أو تحت ضغط، كما يحدث أثناء التخفيف أو النقل، فإن إفراز السالمونيلا يزداد بشكل كبير، مما يرفع من احتمال إصابة نسبة أكبر من القطيع مع اقتراب موعد الذبح. ومع ذلك، فإن ذلك لا يعني بالضرورة أن اللحوم أو البيض ستكون ملوثة. ومن خلال التركيز على الحيوان وسلوك البكتيريا داخله، يمكن اتخاذ خطوات تقلل من فاعلية مسار العدوى.
يُعد مسار الانتقال “ناجحًا” عندما تتحول الدواجن أو لحومها إلى إيجابية للسالمونيلا في بيئة تحتوي بالفعل على البكتيريا. ولمنع ذلك، يمكن اعتماد مبدأين رئيسيين: الأول من خلال العمل على البكتيريا بمجرد دخولها إلى الجهاز الهضمي، والثاني هو تعزيز قدرة الحيوان على الدفاع عن نفسه من خلال تقوية جهازه المناعي.
ويُعد S-prove، وهو مكوّن علفي وظيفي من إنتاج شركة Agrifirm، مثالًا على منتج يعمل على كلا المبدأين معًا.
| المعالجة | حمض البيوتيريك (0.03%) | S-prove (0.03%) |
|---|---|---|
| نسبة القتل | 70,0 | 97,64 |
| نسبة البقاء | 30,0 | 2,36 |
| كفاءة الغزو | 4,35 | 1,69 |
| الخطر الإفتراضي لتلوث السالمونيلا | 1,31 | 0,04 |
فعالية مؤكدة ضد السالمونيلا بفضل تأثيراته المباشرة و غير المباشرة المضادة للبكتيريا: S-Prove
يتمتع S-prove بنشاط قوي مضاد للبكتيريا تجاه سلالات السالمونيلا، سواء المتخصصة بالمضيف (مثل S. Gallinarum وS. Pullorum) أو غير المتخصصة (مثل S. Enteritidis، وS. Typhimurium، وS. Java، وS. Infantis وغيرها). يعمل S-prove على تدمير غشاء الخلية البكتيرية، مما يؤدي إلى تسرب محتويات الخلية، وبالتالي إضعاف البكتيريا وموتها في النهاية. وبفضل تركيبه، يستطيع S-prove الدخول بسهولة عبر الثقوب الناتجة في الغشاء الخلوي، ويُطلق البروتونات التي تؤدي إلى تحمّض محتوى الخلية، مما يُسارع في القضاء على البكتيريا. وفور انطلاق البروتونات، تتداخل الجزيئات سالبة الشحنة مع الحمض النووي للبكتيريا، مما يمنعها من تكرار نفسها قبل أن تموت.
يساهم التأثير المضاد للبكتيريا الذي يتمتع به S-prove، إلى جانب قدرته على الحد من تكاثر البكتيريا، في تقليل إفراز السالمونيلا عبر البراز، مما يقلل من الحمل البكتيري الكلي في عنبر الدواجن، وبالتالي يقلل من خطر التلوث المتبادل بين الطيور.
وبالإضافة إلى هذا التأثير المباشر على بكتيريا السالمونيلا، فإن S-prove يؤثر كذلك على التعبير الجيني المرتبط بعوامل الفوعة (العدوانية) لدى البكتيريا، مما يقلل بشكل كبير من قدرتها على غزو مجرى الدم والانتقال إلى أعضاء أخرى خارج الجهاز الهضمي. وبهذا الشكل، يساعد S-prove أيضًا في منع تلوّث العضلات والأعضاء الداخلية قبل الحصاد.
أظهرت الدراسات المختبرية (in vitro) والدراسات خارج الجسم الحي (ex-vivo) أن هذا النهج يمكنه أن يوقف مسار انتقال السالمونيلا بنسبة تصل إلى 99.9% (انظر الجدول 1).
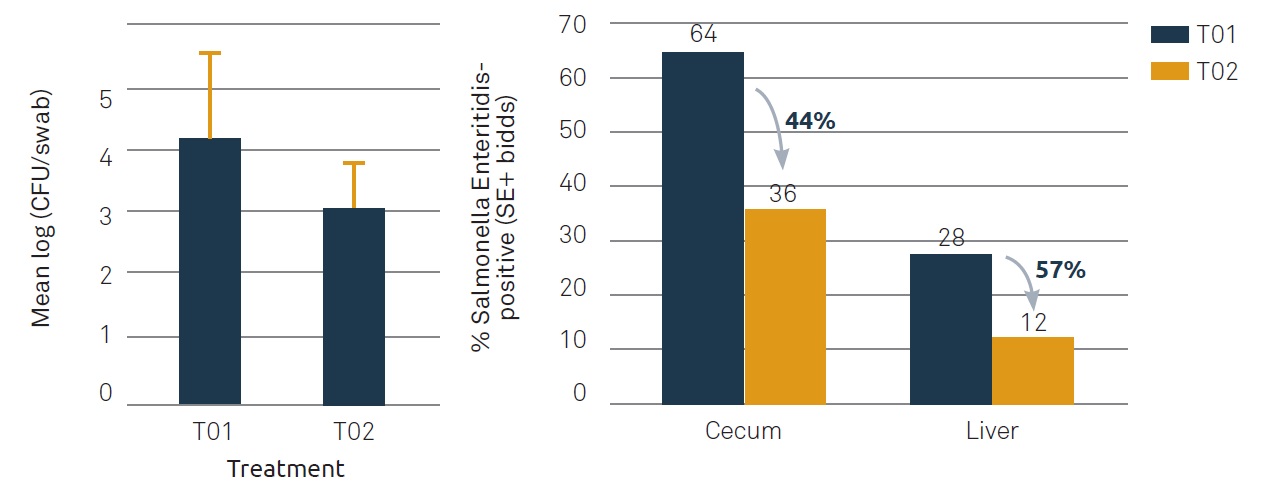
أما في الدراسات داخل الجسم الحي (in vivo)، فقد أظهرت تجربة تحدٍّ تم فيها إصابة الطيور بالسالمونيلا Enteritidis في اليوم السابع بتركيز 1.6 × 10³ وحدة CFU/طائر، أن S-prove، عند استخدامه حتى اليوم الثاني عشر، قادر على تقليل وجود السالمونيلا في مسحات المجمع (cloacal swabs) للطيور (بحسب متوسط اللوغاريتمات، p<0.053)، كما قلّل عدد الطيور التي أظهرت نتائج إيجابية في محتوى الأعور بنسبة 44%، وعدد الطيور التي ظهرت فيها السالمونيلا في الكبد (ما يشير إلى حدوث غزو فعلي) بنسبة 57% مقارنة بالمجموعة الضابطة (انظر الشكل 2).
تُؤكد هذه الأبحاث أن الدواجن تمتلك القدرة على مقاومة التلوث بالسالمونيلا، كما تُظهر أن منتج S-prove قادر على خفض نسبة تلوث الأعضاء (سواء اللحوم أو البيض) بالسالمونيلا من 57% إلى 12%. وبعيدًا عن تأثيره المباشر على البكتيريا، كيف يتمكن S-prove من تحقيق هذا التأثير الكبير في تقليل انتقال العدوى إلى الحيوان؟
السبب الرئيسي يعود إلى تنشيط الاستجابة المناعية الخلوية (cell-mediated) والخلطية (humoral) التابعة لكل من الجهاز المناعي الفطري والمكتسب. تلعب الخلايا الكأسية (Goblet cells)، المسؤولة عن إفراز المخاط، دورًا رئيسيًا في خط الدفاع الأول، حيث تقلل من قدرة السالمونيلا على الالتصاق بالخلايا الظهارية. ومع زيادة عدد هذه الخلايا نتيجة استخدام S-prove، تتراجع قدرة البكتيريا على الالتصاق بالغشاء المعوي، ومن ثم اختراقه والانتقال إلى مجرى الدم أو الأعضاء الأخرى.
تمتلك الدواجن القدرة على إفراز مادة بيتا-ديفينسين 9 (β-defensin 9) الخاصة بالطيور، وهي ببتيد مضاد للميكروبات يعمل على قتل السالمونيلا ضمن آليات كل من الجهاز المناعي الفطري والمكتسب. ويتم إفراز هذا الببتيد بشكل أساسي من الطحال، وقد ثبت أن S-prove يُحفّز إفرازه بشكل كبير، مما يُعزز من النشاط المضاد للبكتيريا داخل جسم الطائر.
وقد أظهرت أبحاث أُجريت في جامعة الطب البيطري في فيينا أن S-prove يزيد من عدد الخلايا التائية (T-cells)، حيث ارتفعت أعداد كل من الخلايا CD4+ وCD8+، لكن الزيادة الأهم كانت في الخلايا السامة المنشطة CD8CD25، ما يشير إلى أن الاستجابة المناعية الخلوية التكيّفية أصبحت أكثر قدرة على تدمير الخلايا المصابة بالبكتيريا.
وبالإضافة إلى هذا الدور التدميري المباشر، تقوم الخلايا CD4+ بتحفيز إفراز العديد من السيتوكينات الالتهابية عند الحاجة، مما يتيح استجابة أسرع وأكثر فاعلية ضد الأجسام الغريبة. وعلى الرغم من أن الخلايا التائية تنتمي إلى الجهاز المناعي المكتسب، إلا أنها تُعد أيضًا حلقة وصل مهمة تربط بين الجهازين الفطري والمكتسب.
وقد أثبتت دراسة سابقة أجراها وانغ وآخرون عام 2023 أن الدواجن التي تتمتع بنسبة منخفضة من H/L (نسبة الخلايا غير المتجانسة إلى اللمفاوية – أي الفطرية إلى التكيّفية) تُظهر مقاومة أعلى لعدوى السالمونيلا.
الخاتمة
لا يمكن تحقيق الوقاية الفعالة من تلوث السالمونيلا إلا من خلال تحديد دقيق للمخاطر، لتحديد المصادر الأساسية للتلوث أو إعادة التلوث—سواء داخل عنابر الدواجن أو في البيئة المحيطة بها. التركيز فقط على الأنشطة أو الحيوانات التي قد تشكل خطرًا لا يكفي للحد من انتشار الطيور المصابة بالسالمونيلا في نظامك الإنتاجي. بل إن العمل على كسر مسار انتقال العدوى من خلال تعزيز المقاومة الطبيعية للدواجن ضد التلوث، وتحفيز النشاط المضاد للبكتيريا داخل أجسامها، يُعد أمرًا بالغ الأهمية في حماية المنتج، والمحافظة على سمعة علامتك التجارية، وضمان استمرارية الربحية.